金沢大学新学術創成研究機構の小川数馬教授,三代憲司准教授,大学院医薬保健学総合研究科薬学専攻/次世代精鋭人材創発プロジェクト令和 4 年度採用選抜学生(博士課程 3 年)の越後拓亮,医薬保健研究域薬学系の淵上剛志准教授,宗兼将之助教,福島県立医科大学の高橋和弘教授,鷲山幸信准教授,金沢大学附属病院核医学診療科の絹谷清剛教授,若林大志講師らの共同研究グループは,標的 α 線治療(※1)のがん選択的な治療を可能とする手法の開発に成功しました。
核医学治療に用いられる α 線は高い細胞傷害性を持ち,飛程が短いことから,α 線放出核種をがん細胞に選択的に送達することができれば,少ない副作用で高い治療効果を得ることができます。特にアスタチン-211 (211At)(※2)は,国内での製造方法が確立しているほぼ唯一の α 線放出核種であり,近年,臨床応用に向けた 211At 標識薬剤の開発が盛んに行われています。
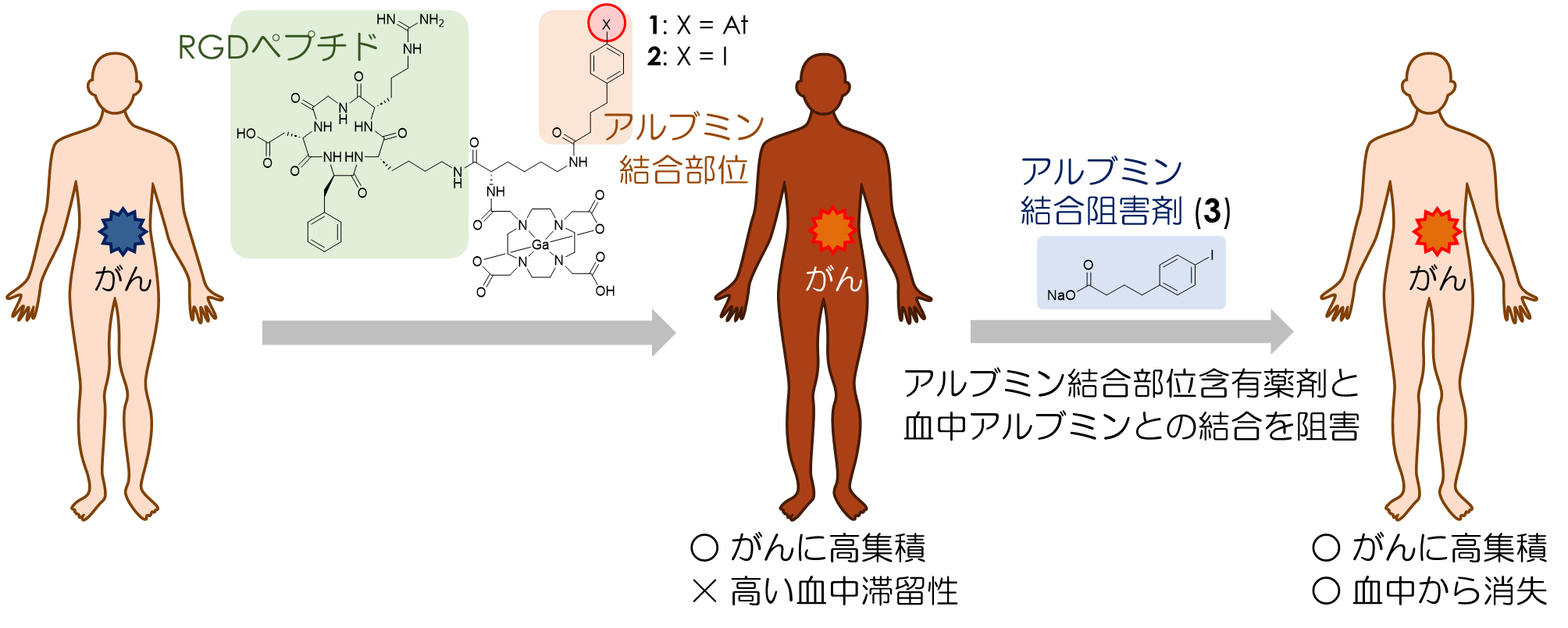
本研究グループは 211At による標的 α 線治療を行うために,これまでの研究において,血液中に豊富に存在するタンパク質であるアルブミンに結合する薬剤 ([211At]1) を開発し,マウスでの実験で[211At]1 ががんに高く集まり,がんの増殖を抑制することを示しました。しかし,[211At]1 が血液中に長く滞留することから副作用が懸念されていました。そこで,十分量の[211At]1 をがんに運んだ後、[211At]1 と血中アルブミンとの結合を切る化合物 (3) を追加で投与することで、[211At]1 のがんへの選択性を改善可能か検討を行いました。 その結果,[211At]1 は血液中に滞留することなく,がん以外の正常な組織からも速やかに排泄されました。一方,がんへの集積はあまり低下せず,がんの増殖を抑制しました。このことから本研究をさらに発展させることにより,標的 α 線治療のさらなる効果増大,副作用の低下につながることが期待されます。
本研究成果は,2024 年 4 月 4 日欧州核医学会が出版する国際誌『European Journal of Nuclear Medicine and Molecular Imaging』のオンライン版に掲載されました。
図:本研究の概念図
【用語解説】
※1:標的 α 線治療
がん細胞を殺傷する α 線を放出する核種で,がん細胞に選択的に集積する化合物を標識された薬剤を患者さんに投与し,体内からがん細胞を殺傷する治療法。α 線は β−線より飛程が短く,細胞傷害性が大きいため,少ない副作用で高い治療効果が得られる。
※2:アスタチン-211(211At)
α 線放出核種であり,高い細胞傷害性を示すことから,強力ながん治療効果が期待されている。アスタチンには安定同位体が存在しないが,ハロゲン元素であるため,ヨウ素や臭素など他のハロゲン元素と類似した化学的性質を持ち,既知の標識法を応用できる。
ジャーナル名:European Journal of Nuclear Medicine and Molecular Imaging
研究者情報:小川 数馬




 PAGE TOP
PAGE TOP