金沢大学先進予防医学研究センターの斎藤洋平助教、医薬保健総合研究科創薬科学専攻の田部井透矢(研究当時)、医薬保健研究域薬学系の後藤(中川)享子教授らの研究グループは、ホウ素キレート(※1)化合物を利用した新たな標的同定法の開発に成功しました。
医薬品の開発や生命現象の解明には、生物活性化合物(※2)が作用するタンパク質(標的)を明らかにする必要があります。その手法として広く利用されているのが、担体にリンカー(※3)を介して化合物を固定化後、標的となるタンパク質を捕捉し、リンカーを切断することで捕捉したタンパク質を溶出するというものです。しかしながら、既存の方法ではリンカーの切断が容易ではなく、さまざまな試薬を利用する必要があり、標的タンパク質の直接的な機能解析が困難である等の問題点が多く顕在するため、画期的手法の開発が求められていました。
本研究グループは、ホウ素原子がアミノ酸とキレート化合物(ボロキサゾリドン)を形成可能な点に着目してリンカーとしての応用を試み、生体高分子(※4)存在下でも利用可能な温和な条件でボロキサゾリドンの形成ならびに解離に成功しました。本方法の有用性を実証するために、ボロキサゾリドンの形成を介してビオシチン(※5)を担体に固定化後、効率的なアビジン(※6)の捕捉、さらに温度制御のみでリンカーを解離させビオシチン–アビジン複合体を溶出することにも成功しました。本結果は、問題点の一つであるリンカーの切断効率を大幅に改善できる可能性があります。切断に特別な試薬を必要とせず、温和な温度制御のみで自在に標的タンパク質を溶出でき、標的タンパク質の機能解析をも可能にすることから、これまでにない斬新な標的同定法と言えます。
本研究で得られた知見は将来、創薬研究における治療標的の同定や生命現象を司る重要因子の解明に活用されることが期待されます。
本研究成果は、2024年11月8日9時(ロンドン時間)に英国王立化学会が出版する国際学術誌『Chemical Communications』のオンライン版に掲載されました。
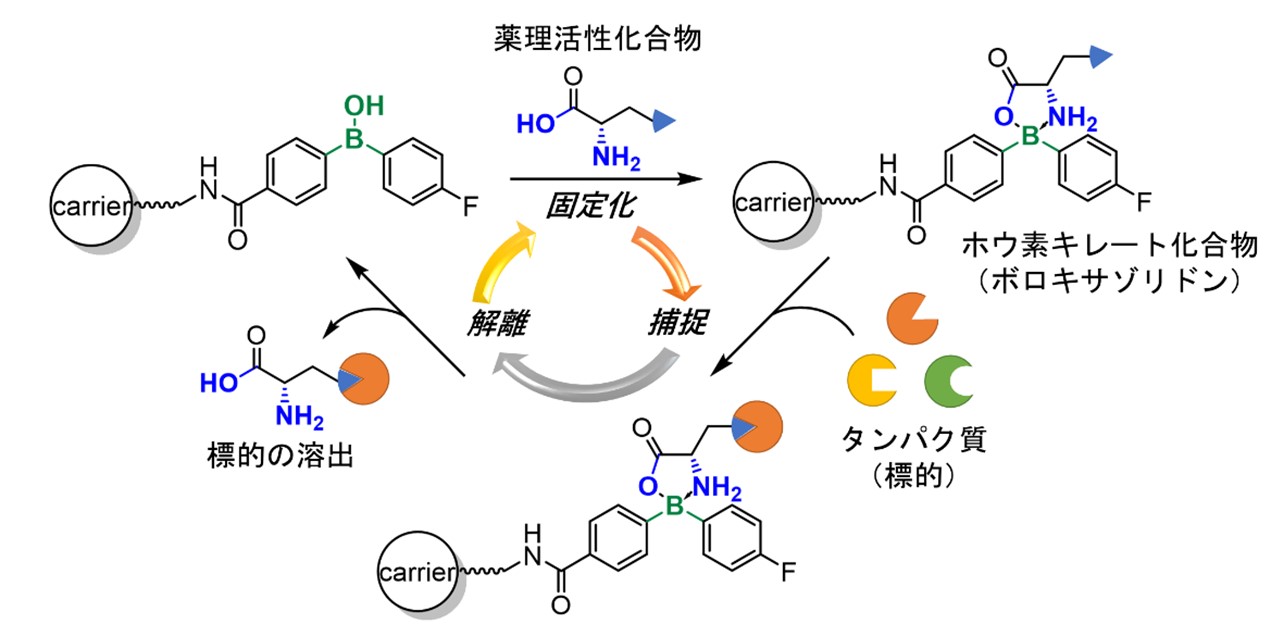 本研究の概要図
本研究の概要図
【用語解説】
※1:ホウ素キレート
ホウ素原子に対する配位結合により生じる構造の総称。
※2:生物活性化合物
医薬品や毒のように、生物の体内でタンパク質や酵素等と相互作用して特定の効果を示す化合物。薬として作用するものを、特に、薬理活性化合物という。
※3:リンカー
担体と化合物を繋ぐための架橋構造。
※4:生体高分子
タンパク質や核酸など生体内に存在する高分子量の有機化合物。
※5:ビオシチン
水溶性ビタミンの1種であるビオチンにアミノ酸のリシンがε位で結合した分子。ここでは薬理活性物質の代替として使用。
※6:アビジン
卵白中に存在する塩基性の糖タンパク質。ビオチンの標的タンパク質。
ジャーナル名:Chemical Communications
研究者情報:斎藤 洋平




 PAGE TOP
PAGE TOP