金沢大学医薬保健研究域薬学系(薬物動態学)の中西猛夫准教授,玉井郁巳教授,大学院医薬保健総合研究科博士後期課程の中村吉伸らの研究グループは,帝京大学薬学部の出口芳春教授らとの共同研究により,脳の視床下部の体温調節中枢に作用し体温を上昇させるプロスタグランジンE2(PGE2)の濃度が,プロスタグランジントランスポーター(OATP2A1/SLCO2A1)(※1)によって制御されることを明らかにしました。
これまで,ウイルスや細菌などの微生物が体内に侵入すると,発熱メディエータとして情報を伝達するPGE2が脳内で盛んに産生されることが知られていましたが,細胞内で作られたPGE2がどのように分泌されるかについては十分に解明されていませんでした。
今回,本研究グループは,PGE2の運び屋であるOATP2A1遺伝子を全身から欠損したマウス(OATP2A1全身ノックアウトマウス)に発熱物質を投与し,その結果,その体温上昇がほぼ完全に抑制されることが明らかになりました(図1)。また,同マウスではPGE2濃度が低値を示していることから,OATP2A1は,PGE2の産生源である脳内ミクログリア(※2)や血管内皮細胞で強く発現することを見いだしました(図2)。
これらの事実は,OATP2A1が発熱物質の侵入に伴い産生されるPGE2を脳内に分泌し,発熱反応のスイッチをONにする分子スイッチとして機能することを示唆しています(図3)。PGE2は起炎物質・発痛増強物質であると同時に,生命維持に欠かせない多様な役割を担います。現在,主に使用されているPGE2合成阻害を機序とする抗炎症薬にはしばしば重篤な副作用が伴います。今回の発見により,OATP2A1を標的とし,PGE2合成を阻害しない新しい解熱・鎮痛薬の開発につながることが期待されます。
本研究成果は,2018年5月21日(米国東部標準時間)に北米神経科学学会誌『The Journal of Neuroscience』のオンライン版に掲載されました。
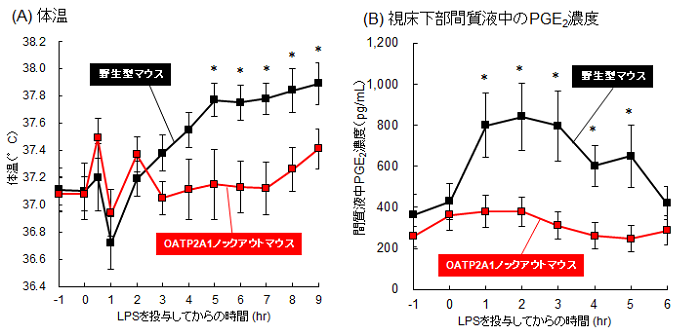
図1 体温および脳の間質液中PGE2濃度に対するOATP2A1遺伝子欠損の影響
外因性発熱物質であるリポポリサッカライド(LPS)の投与後,OATP2A1全身ノックアウトマウスでは,体温(A)および脳間質液PGE2濃度(B)が変化しない。
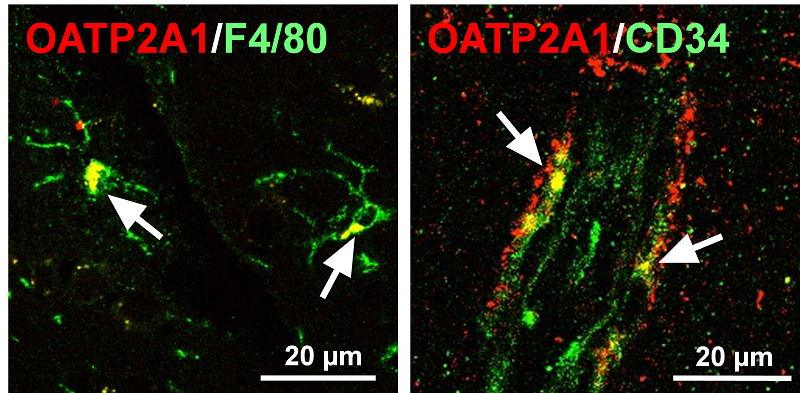
図2 マウス脳ミクログリア(左)および血管内皮細胞(右)におけるOATP2A1の発現
矢印(黄色)はOATP2A1(赤色)とミクログリア(F4/ 80)または血管内皮細胞マーカー(CD34,緑色)のタンパク質発現部位が一致することを示す。
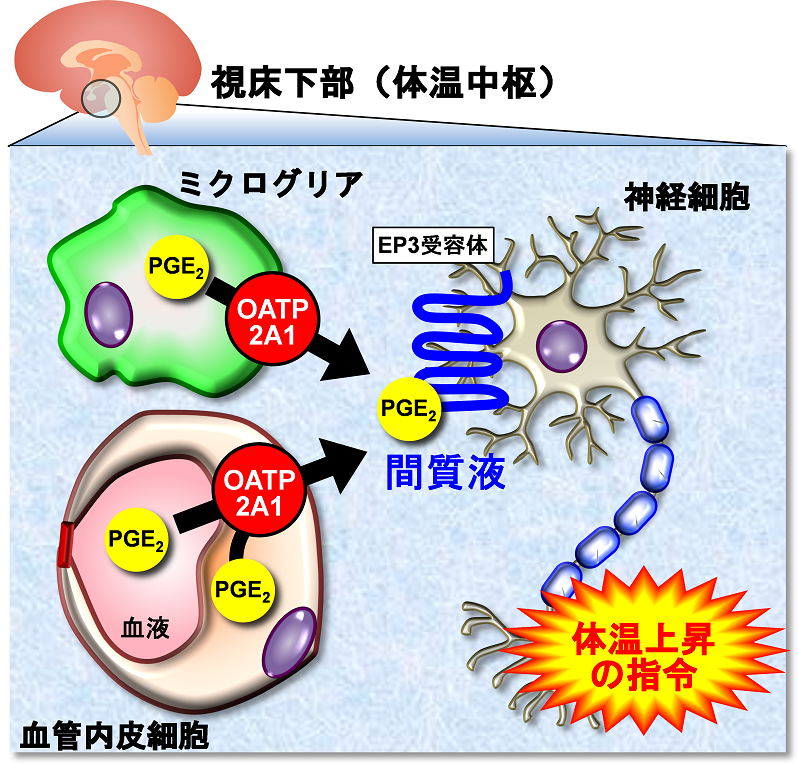
図3 OATP2A1による視床下部(体温中枢)におけるPGE2濃度と体温調節
OATP2A1はミクログリアや血管内皮細胞の細胞内で合成されたPGE2の分泌,あるいは血液中PGE2の脳内への供給に働き,視床下部間質液中のPGE2濃度を維持することで発熱調節に関わる。
【用語解説】
※1 プロスタグランジントランスポーター(OATP2A1/SLCO2A1)
有機アニオン輸送ポリペプチドの一種で,PGE2などを輸送する膜タンパク質輸送体。
※2 ミクログリア
中枢神経系グリア細胞の一つで,中枢神経系に常在するマクロファージ。




 PAGE TOP
PAGE TOP